W artykule przedstawiono kształtowanie się zmian ciśnienia i dekompresji, zjawisk fizycznych będących przedmiotem zainteresowania i badań medycyny lotniczej i kosmicznej. Ujednolicono poglądy na parametry fizyczne pozwalające ocenić dekompresję i jej skutki dla ustroju, określono również zmiany wywołane dysbaryzmem i ebulizacją płynów ustrojowych.
W artykule przedstawiono również współczesne poglądy na etiologię i patogenezę choroby dekompresyjnej, jej podziały oraz czynniki usposabiające do jej wystąpienia. Przedstawiono także metody postępowania profilaktycznego w warunkach, kiedy może dojść do wystąpienia choroby dekompresyjnej.
Dekompresja
Zmianę ciśnienia z wysokiego do ciśnienia niskiego nazywamy dekompresją (zmiana ciśnienia z niskiego do wysokiego nosi nazwę - rekompresji). Przyjęto rozróżniać:
- dekompresję nagłą (gwałtowną, eksplozywną), jeżeli zmiana ciśnienia następowała w czasie poniżej jednej sekundy,
- dekompresję umiarkowaną, jeżeli zmiana ciśnienia następowała w czasie poniżej jednej minuty,
- dekompresję powolną [15].
Właściwie jednak nie ma jednoznacznego i ogólnie przyjętego kryterium dla określenia zjawiska nagłej dekompresji. Ważną rolę w ocenie nagłej zmiany ciśnienia z wysokiego do niskiego odgrywają niżej przedstawione parametry fizyczne, za pomocą których ocenia się to zjawisko. Są to wysokość nad poziomem morza, na której nastąpiła zmiana ciśnienia, oraz fizjologiczny stan ustroju, np. wielkość ciśnienia wewnątrzpłucnego w czasie dekompresji, o którego roli będzie mowa w dalszej części pracy (w organizmie, w którym nie stwierdza się zmian patologicznych).
Zmiana ciśnienia, zwana dekompresją, występuje nie tylko w lotnictwie, gdzie najczęściej jego przyczyną jest nagłe, awaryjne rozszczelnienie kabiny samolotu, lecz również w pracy nurków (zmiany ciśnienia liczone nawet w atmosferach) i to zarówno nurków zawodowych, jak i u ludzi uczestniczących w coraz popularniejszym nurkowaniu sportowym. Z dekompresją mogą się spotkać budowniczowie metra, gdzie zwykle przy tarczy drążącej, w tzw. „przodku", zwiększa się ciśnienie zapobiegające w jakimś stopniu wyciekowi wody, w łodziach podwodnych, górnictwie, spadochroniarstwie itp. [5, 12, 13]. W przedstawionym opracowaniu zmiany ciśnienia, dekompresji, dysbaryzmu i choroby dekompresyjnej odniesiono tylko do warunków jakie mogą wystąpić w lotnictwie i ewentualnie w medycynie kosmicznej.
Ogólnie uważa się, że nagłą dekompresją określamy zjawisko wyrównywania się ciśnienia gazów z wyższego do niższego, w czasie poniżej jednej sekundy, oraz wtedy, gdy to zjawisko może spowodować wzrost ciśnienia wewnątrzpłucnego więcej niż o 20-30 mm Hg. W lotnictwie [15, 18] uważa się również, że mamy do czynienia ze zjawiskiem nagłej dekompresji kiedy:
-współczynnik ucieczki gazu (wielkość otworu do objętości kabiny) jest wyższy od 1/100 m2/m3
-kiedy współczynnik względnego ciśnienia (stosunek ciśnienia początkowego do ciśnienia końcowego) jest wyższy od 2,3.
Wraz ze zmianą ciśnienia zwiększa się objętość gazów. Według prawa Boyle-Mariotte'a objętość danego gazu zwiększa się proporcjonalnie do obniżenia ciśnienia. Żywy ustrój zawiera substancje gazowe bądź jako gaz wolny, bądź w postaci rozpuszczonej. Podczas zmiany ciśnienia gaz ten zwiększa swoją objętość wywołując w ustroju cały zespół zaburzeń zwanym dysbaryzmem (w piśmiennictwie spotyka się również określenia tego zjawiska jako meteoryzmu wysokościowego). Dysbaryzmem nazywamy więc zespół charakterystycznych zaburzeń związanych ze zmianą objętości gazów ustroju wskutek obniżenia ciśnienia w otaczającej atmosferze. Po raz pierwszy termin ten został wprowadzony w Stanach Zjednoczonych [10, 11]. Zależnie od charakteru i umiejscowienia zespołu objawów, w ustroju poddanym zmianie ciśnienia z wysokiego do niskiego - zwanego dekompresją - wyróżniamy:
- aerosinusitis - lotnicze zapalenie zatok,
- aerodentalgie - bóle zębowe u pilotów,
-aerotitis media - lotnicze zapalenie ucha środkowego,
- niedostateczną barofunkcję - zmiany w uchu środkowym lub w zatokach obocznych nosa wywołane niedostatecznym wyrównywaniem się ciśnienia z otaczającą atmosferą,
- zjawiska meteoryzmu (dysbaryzmu) w jamie brzusznej - dolegliwości w jamie brzusznej spowodowane rozszerzającym się gazem w przewodzie pokarmowym. W wypadku, gdy dekompresja wystąpiła na wysokościach, gdzie ostateczne ciśnienie otaczającej atmosfery osiąga wartości poniżej 47 mm Hg, mamy do czynienia ze zjawiskiem ebulizacji - wrzenia płynów ustrojowych (ciecz o temperaturze 37°C w ciśnieniu 47 mm Hg - wrze).
W zależności od tego, gdzie wtedy gromadzi się para wodna (wskutek gwałtownego parowania płynów ustrojowych) mamy do czynienia z:
- vapothoraxem - para wodna w klatce piersiowej,
- vapoperitoneum - para wodna w jamie brzusznej,
- vapopericardium - para wodna w worku osierdziowym.
Należy dodać, że wrzenie płynów zaczyna się w ustroju tam, gdzie jest fizjologicznie najniższe ciśnienie - w prawej połowie serca.
Dla oceny zjawiska nagłej dekompresji, przewidywania wystąpienia możliwych zmian patologicznych w ustroju, ich umiejscowienia i wielkości, rokowania i postępowania lekarskiego stosuje się wymienione parametry fizyczne, określające zjawisko dekompresji:
1. Czas nagłej dekompresji (t), w sekundach lub milisekundach.
2. Wielkość nagłej dekompresji (ΔP) - różnica między ciśnieniem początkowym (Δp) a ciśnieniem końcowym (Δk)
ΔP = Δp - Δk
3. Szybkość nagłej dekompresji (V)
V = ΔP /1
4. Iloraz nagłej dekompresji (E)
E = Δp / Δk
5. Współczynnik ucieczki gazu (F)
F=(V/A)*C
gdzie: V - objętość kabiny, A - powierzchnia otworu, C - szybkość dźwięku.
6. Wielkość ciśnienia końcowego - ΔPk.
Każdy z parametrów przedstawionego wyżej wzoru wymaga wnikliwej analizy, ale wnioski końcowe są istotne jedynie, po wzięciu pod uwagę wszystkich parametrów fizycznych określających analizowaną dekompresję. Na przykład, nawet niewielka delta dekompresji określająca różnicę między ciśnieniem początkowym a końcowym, zaistniała w milisekundach, może uczynić znaczne szkody w ustroju, w porównaniu do dekompresji z większą różnicą ciśnień, lecz przebiegającą wolniej, a więc taką, w której istnieje pewien margines czasu pozwalający w jakimś stopniu wyrównywać ciśnienie wnętrza ustroju z ciśnieniem otaczającym.
Z kolei wielkość nagiej dekompresji przekraczająca wartość ok. 1/3 ciśnienia jednej atmosfery, może być dla człowieka również bardzo niebezpieczna. Stąd w kabinach samolotów bojowych ciśnienie jest regulowane tak, aby w przypadku zaistnienia nagłej dekompresji różnica ciśnień nie przekraczała wielkości ok. 1/3 atmosfery (250-260 mm Hg).
Specjalnie wnikliwej oceny wymaga analiza wielokrotności nagłej dekompresji. Wielokrotność (iloraz) nagłej dekompresji z ciśnienia wyjściowego 760 mm Hg do 127 mm Hg wynosi ok. 6. Dekompresja z ciśnienia 380 mm Hg do ciśnienia końcowego 63 mm Hg, to również wielokrotność ok. 6. Jednak olbrzymia różnica ciśnień określająca wielkość dekompresji w pierwszym przypadku, w stosunku do drugiej dekompresji wskazuje, gdzie mogłyby wystąpić większe uszkodzenia organizmu.
We wstępie przedstawiono, między innymi, że wystąpienie zmian patologicznych w organizmie w czasie nagłej dekompresji zależy również od objętości gazów w płucach (Vpp). Wielkość gazów w płucach uzależniona jest z kolei od fazy oddychania, w której nastąpiła dekompresja i wielkości oporu prądu powietrza w drogach oddechowych. Według wielu autorów uważa się, że uszkodzenia tkanki płucnej powstają przy nagłym wzroście ciśnienia w płucach w granicach od 50-80 mm Hg [2, 5, 15]. Jest to duży przedział wartości ciśnienia uznawanego za szkodliwe. Różnice w poglądach na wielkość uszkadzającą ciśnienia wynikają prawdopodobnie z różnych metod jakie stosowano w przeprowadzonych badaniach (badania przeprowadzano zwykle z udziałem różnych zwierząt). W Polsce przyjęto, że uszkodzenia tkanki płucnej, przy nagłym wzroście ciśnienia w klatce piersiowej, występują przy ciśnieniu ok. 60 mm Hg [10]. Wysokość tego ciśnienia określa się według wzoru:
Pkrytyczne=(Vpp/Vmax )*(Pp- 47 ) + (47 - Pk)
gdzie: Vpp - objętość gazów w płucach przy nagłej dekompresji, Vmax - maksymalna objętość nieuszkodzonych płuc, Pp - początkowe ciśnienie w kabinie, Pk — końcowe ciśnienie w kabinie - równe ciśnieniu otaczającemu.
W związku z tym, że przy nagłej zmianie ciśnienia objętość płuc, oznaczona jako Vpp, ma wpływ na wielkość zwiększonego ciśnienia wewnątrzpłucnego zarówno w piśmiennictwie anglosaskim, jak i rosyjskim, objętość płuc (Vpp) przy nagłej dekompresji przyjęto określać w trzech różnych wielkościach:
- w warunkach pełnego wdechu, kiedy Vpp/Vmax = 1,0;
- w końcu zwykłego wydechu, kiedy Vpp/Vmax = 0,55;
- przy pełnym wydechu, kiedy Vpp/Vmax = 0,25.
Warianty te wynikają z prawa Boyle-Mariottea i przy ocenie tej objętości bierze się pod uwagę wielkość ciśnienia pary wodnej w temperaturze ciała (współczynnik zmiany objętości - BTPS).
Wykorzystując powyższy wzór można obliczyć wielkość zwiększonego ciśnienie w płucach przy nagłej dekompresji, przy różnych wielkościach ciśnienia w kabinie i przy różnych objętościach powietrza w płucach. W.B. Małkin [15] przedstawił wielkości zwiększonego ciśnienia w płucach w zależności od wielkości ciśnienia w kabinie (przy zamkniętej głośni), w wypadku nagłej dekompresji.
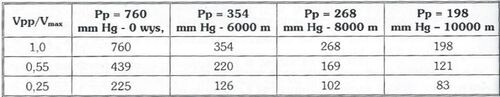
Jak wynika z danych zwartych w tej tabeli, wielkość ciśnienia wewnątrzpłucnego (przy zakrytej głośni) we wszystkich przypadkach wielkości ciśnienia w kabinie przewyższa, w wypadku nagłej dekompresji, krytyczną wielkość dla płuc przyjętą w Polsce (60 mm Hg), lecz również i wielkość uznawaną przez innych autorów (80 mm Hg) [2, 5]. Zamknięta głośnia, w warunkach nagłej dekompresji, to najgorszy wariant dla przewidywanych uszkodzeń w ustroju. Jeżeli powietrze w jakimś stopniu uchodzi i ciśnienie w kabinie wynosi ok. 268 mm Hg, mniejsze jest prawdopodobieństwo uszkodzenia płuc.
Maksymalną wielkość wzmożonego ciśnienia wewnątrzpłucnego w czasie nagłej dekompresji można również określić według wzoru przedstawionego w 1973 r. przez J.Boyle [2] (autor określając maksymalne ciśnienie wewnątrzpłucne w czasie nagłej dekompresji zakłada, że następuje ono w momencie wyrównywania się ciśnienia z otaczającym). Wyniki licznych prac eksperymentalnych (między innymi z udziałem ludzi) potwierdzają słuszność przedstawionego równania.
ΔPmaks. = {( Pp - 47)*(Vi/Vmax) +47 - Pk } * (1 –(tcc /tc ))
Wyrażenie: (1 –(tcc /tc )) jest oryginalnym opracowaniem Boyle'a i jest czynnikiem rozróżniającym szybkość dekompresji w kabinie - tcc i w płucach tc.
Wyniki badań doświadczalnych (na szczurach) wykazały, że śmierć ok. 10% badanych zwierząt stwierdza się przy dekompresji z ciśnienia 622 do 62 mm Hg.
Iloraz nagłej dekompresji (E) ok. 10. Warunki takie występują, gdy stosunek V/A wynosi 3,3 m3/m2. W przypadkach, gdy V/A wynosi 1,2 m3/m2 ginie ok. 50% zwierząt, zaś gdy V/A równe jest 0,12 m3/m2 - ginie 100% zwierząt. Krwotoki w płucach obserwowano przy nagłej dekompresji, gdy objętość płuc powiększała się ok. 2,3-2,5 razy. Przy trzykrotnym powiększeniu objętości płuc obserwowano ich rozerwanie.
We własnych badaniach ludzi w warunkach nagłej dekompresji wielkości 150 mm Hg i szybkości 0,34 sekundy (dekompresja była wykonywana w czasie wydechu), obserwowano znaczne zaburzenia fizjologicznego rytmu oddychania [8, 16]. Rycina 1 ilustruje zmiany krzywej oddychania w czasie dekompresji. Strzałka wskazuje moment doświadczalnej dekompresji.
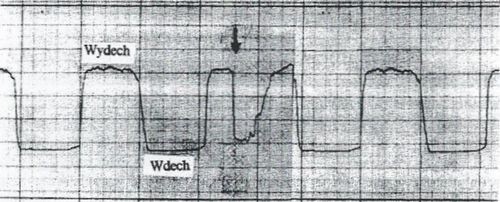
Badani stwierdzali, że w czasie dekompresji odczuwali ucisk w klatce piersiowej i nagłe wydostawanie się powietrza przez nos i usta i mimo tej ucieczki powietrza pojawiało się uczucie potrzeby wykonania jeszcze głębokiego wydechu. W czasie nagłej dekompresji, w warunkach, kiedy występuje duży wzrost ciśnienia wewnątrz-płucnego, obserwuje się również zmiany w układzie krążenia. Zmiany te, to krótkotrwały wzrost a następnie duży spadek ciśnienia tętniczego skurczowego i rozkurczowego krwi oraz zwolnienie a następnie przyśpieszenie częstości skurczów serca. Zmiany takie są spowodowane odruchem płucno-sercowym, w którym dużą rolę odgrywa nerw błędny. Badania wykazały, że obustronne przecięcie nerwów błędnych znosi przedstawioną reakcję układu krążenia w czasie nagłej zmiany ciśnienia. Oczywiście, zawsze możliwe jest, w warunkach nagłej dekompresji, mechaniczne uszkodzenie mięśnia sercowego i naczyń krwionośnych.
Nagła dekompresja doprowadza do powstania napięcia emocjonalnego i pojawienia się odpowiednich reakcji ruchowych. W przypadkach, gdy nie występuje uszkodzenie tkanki płucnej, czy też innych tkanek, dekompresja zawsze ma określony wpływ na ogólne samopoczucie i zdolność do pracy [1, 11].
Meteoryzm wysokościowy
Poza powietrzem w płucach, w przewodzie pokarmowym znajduje się również gaz powstały w procesie fermentacji, w ilości od 500 do 1 500 ml. Gaz znajduje się również w zatokach przynosowych (ok. 35 ml) i w uchu środkowym (ok. 11 ml). Przy obniżeniu się ciśnienia otaczającego zwiększa się objętość gazów.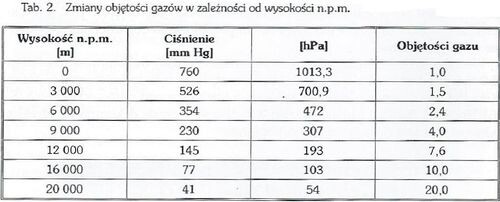
Rozszerzenie się gazów pod wpływem nagłej dekompresji, w obrębie jamy brzusznej może spowodować wzdęcie brzucha i wystąpienie dolegliwości bólowych. Dolegliwości te zależą od ilości gazów, ich lokalizacji i możliwości wyjścia z jelit. Rozszerzenie odcinków jelit zawierających gaz powoduje odruchowy skurcz sąsiednich odcinków jelit, co utrudnia przemieszczanie się gazów. W skrajnych przypadkach może dojść do uszkodzenia przewodu żołądkowo-jelitowego. Ogólnie określa się, że zmiany w przewodzie pokarmowym zależą od jego stanu anatomicznego i czynnościowego, rodzaju diety, czasu jaki upłynął od spożycia posiłku, stopnia napięcia powłok brzusznych itp. Przyjmuje się, że próg bólowy ciśnienia, pod wpływem wzrostu objętości gazów w przewodzie pokarmowym, wynosi: dla jelita cienkiego - 80-100 mm Hg, jelita grubego - ok. 40 mm Hg, żołądka - ok. 20 mm Hg.
Meteoryzm wysokościowy może powodować, na drodze odruchowej, zaburzenia w układzie krążenia, takie jak skurcze przedwczesne, bradykardia i zapaść. Obserwuje się też inne zmiany związane z zaburzeniami czynności układu autonomicznego jak: wzmożona potliwość, zaczerwienienie lub zblednięcie.
Ciężkie stany patologiczne, spowodowane meteoryzmem wysokościowym spotyka się raczej rzadko. Zgodnie z danymi amerykańskimi, na prawie 5 000 przypadków, w których wystąpiły dolegliwości związane z meteoryzmem wysokościowym, ciężkie stany patologiczne obserwowano tylko u 12 osób [6, 17].
Wcześniej przedstawiono, że objawy dysbaryzmu mogą występować także w postaci bólów w uszach, zatokach obocznych nosa i zębów. Przy niesieniu pomocy, w przypadkach związanych z zaburzeniami spowodowanymi wysokościowym meteoryzmem, poszkodowanych należy jak najszybciej umieścić w normalnym środowisku gazowym.
Choroba dekompresyjna
Zespół objawów, powstających wskutek działania gazu przechodzącego ze stanu rozpuszczenia w stan gazowy, w warunkach zmiany ciśnienia otaczającego z wysokiego do niskiego, obejmujemy ogólną nazwą „choroby dekompresyjnej". Określenie to zostało w medycynie lotniczej i kosmicznej powszechnie przyjęte i jest obecnie używane. Termin „choroba kesonowa" jest używany w przypadkach, kiedy ciśnienie otaczające obniża się z dużego do ciśnienia atmosferycznego. Używa się więc go w stosunku do nurków, ludzi pracujących w kesonach itp. Wyjaśnianiem charakteru powstawania objawów choroby kesonowej zajmowali się między innymi polscy badacze: J. Swiątecki (1900 r.), F. Sulikowski (1902 r.) oraz A. Huszcza (1915 i 1938 r.) [9].
Tkanki stanowią środowisko przesycone gazami, ale stan taki jest jednak niestabilny. Przy obniżaniu otaczającego ciśnienia istnieje możliwość tworzenia się pęcherzyków gazowych. Skład ich jest podobny do składu powietrza pęcherzykowego w płucach, z wyjątkiem procentowej zawartości tlenu. Wielu autorów uważa, że tlen jest bardzo szybko zużywany przez metabolizm tkankowy i odpowiedzialność za występujące objawy choroby dekompresyjnej ponosi azot.
Przy wytworzeniu się we krwi i tkankach stanu przesycenia gazem, uwolniony gaz skupia się zwykle wokół tzw. zalążków gazowych, które powstają ciągle w ustroju, w procesie przemiany materii. Zalążkiem takim jest zwykle dwutlenek węgla. Na tworzenie się pęcherzyków gazowych ma też wpływ zwiększone napięcie mięśni (obniżone ciśnienie hydrostatyczne przyspiesza tworzenie się pęcherzyków) i miejscowe zaburzenia przepływu krwi. Tworzą się one również w miejscach rozgałęzienia naczyń krwionośnych [3, 20]. W badaniach z płynami biologicznymi i tkankami stwierdzono, że jeżeli nie zawierają one gazowych zalążków, nie powstają pęcherzyki gazowe, nawet przy bardzo dużych zmianach ciśnienia 14].
Ilość azotu rozpuszczonego w tkankach i płynach ustrojowych wynosi ok. 1,0-1,5 l. Ze względu na współczynnik rozpuszczalności azotu wynoszący dla wody 0,012 i dla tkanki tłuszczowej 0,06675, najwięcej rozpuszczonego azotu znajduje się w tkankach bogatych w tłuszcze i lipidy. Pośrednio potwierdza ten fakt krzywa dwufazowości wydalania azotu z ustroju. Azot pochodzący głównie z mięśni ma okres połowiczny wydalania ok. 12-15 minut, zaś pochodzący z tkanek bogatych w tłuszcze i lipidy ok. 90-150 minut.
Na rycinie 2 przedstawiono wydalanie azotu podczas oddychania czystym tlenem, czyli podczas tzw. desaturacji ustroju z azotu, w warunkach normobarii.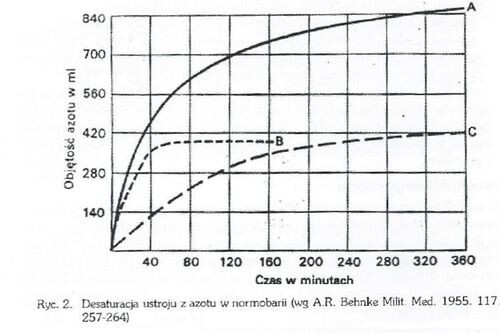
A - wydalanie azotu z całego ustroju, B - wydalanie azotu z płynów ustrojowych, C - wydalanie azotu z tkanki tłuszczowej.
Patogeneza choroby dekompresyjnej
Badania wykazały, że największe skupienia pęcherzyków w chorobie dekompresyjnej spotyka się w żyłach podskórnych, w żyle wrotnej, żyłach wieńcowych serca i żyłach mózgowych. Najwięcej dolegliwości bólowych jest wynikiem działania pęcherzyków gazowych na interoreceptory poza układem krążenia. Dowody na taki punkt widzenia uzasadniają fakt, że [10, 15]:
1) podczas bólu, w chorobie dekompresyjnej brak jest objawów miejscowej sinicy, zblednięcia lub zmiany temperatury (możliwość zmniejszenia przepływu krwi),
2) badania radiologiczne osób z chorobą dekompresyjną wykazały obecność pęcherzyków gazowych w tkance okołonaczyniowej i okołostawowej bez zaburzeń w przepływie krwi,
3) miejscowa rekom presja, okolic bolesnych, znosi bóle nawet podczas wysokich ciśnień w pęcherzykach gazowych,
4) charakter bólów dekompresyjnych jest inny niż bólów anoksemicznych, które są największe podczas czynnego przekrwienia (bóle dekompresyjne w tych warunkach słabną).
Objawy choroby dekompresyjnej są wynikiem zarówno mechanicznego ucisku gazowych pęcherzyków pozanaczyniowych na otaczające tkanki (deformacja, przemieszczenia tkanek, odczucia bólowe), jak i niedokrwienia wywołanego zatorem wewnątrznaczyniowym. Wzajemny wpływ pęcherzyków wewnątrznaczyniowych i zewnątrznaczyniowych można określić za pomocą wzoru [17]:
Pn = H + (2δ/R) + DR
gdzie:
H - hydrostatyczne ciśnienie tkanki (krwi), będącego sumą ciśnienia wewnętrznego (d) i stanu napięcia wewnętrznego tkanki lub ciśnienia krwi (dyn/cm2),
DR - ciśnienie deformujące, które uwarunkowane jest rozmiarami pęcherzyka, jego objętością i właściwościami elastycznymi tkanki (dyn/cm2),
R - ciśnienie otaczające.
Pęcherzyki gazowe, które tworzą się w ustroju, można podzielić na trzy typy (6, 19]:
A) pęcherzyki podstawowe, których ewolucja jest uwarunkowana tylko przemianą gazową z otaczającymi tkankami (dyfuzja),
B) pęcherzyki, których wzrost jest związany nie tylko, z dyfuzją, lecz również z wzajemnym łączeniem się,
C) bezobjawowe pęcherzyki gazowe.
Ewolucja pęcherzyków podstawowych (typ 1) zależy od szybkości przemiany gazowej, między pęcherzykami a otaczającym środowiskiem. Ewolucja rozmiarów pęcherzyków drugiego typu zależy od wielkości ΔP w otaczającym pęcherzyki środowisku. Łączenie się pęcherzyków i ich rozdzielanie jest przypadkowe. Użycie dopplerowskiej metody wykrywania mikropęcherzyków (typ C) w naczyniach krwionośnych, u osób poddanych działaniu dekompresji, jest często wykorzystywane do oceny skutków działania dekompresji wysokościowej i służy do podjęcia decyzji leczenia rekompresją. Rekompresja w atmosferze tlenu jest terapią z wyboru [19].
Nasilenie się występowania mikropęcherzyków w badaniu dopplerowskim ocenia się według 4-stopniowej skali.
I stopień - pęcherzyki gazowe sporadyczne,
II stopień - pęcherzyki wykryte w mniej niż połowie cyklu pracy serca,
III stopień - pęcherzyki wykryte podczas całego cyklu pracy serca,
IV stopień - pęcherzyki wykrywane w sposób ciągły, w czasie rejestracji pracy serca.
Przemieszczanie się pęcherzyków gazowych w czasie występowania choroby dekompresyjnej prowadzi do zmian w rozmieszczeniu się obojętnego gazu (azotu) w organizmie. W tkankach, w których gromadzi się najwięcej pęcherzyków, ogólna zawartość obojętnego gazu sumuje się, wzrastając powyżej przeciętnego średniego poziomu dla danej tkanki. W związku z tym wymywanie go z pęcherzyków jest utrudnione. Taki stan może wpłynąć na niedostateczną skuteczność leczenia wysokościowej choroby dekompresyjnej.
Właściwości struktur tkanek ustroju i związane z tym fizjologiczne i biochemiczne procesy stanowią ważne czynniki, określające szybkość powstawania pęcherzyków, ich rozmiary i pojawienie się wysokościowej choroby dekompresyjnej.
Klinika wysokościowej choroby dekompresyjnej
Powszechnie przyjmuje się, że choroba dekompresyjna występuje najczęściej na wysokościach ok. 9.000 m n.p.m. (230 mm Hg - 307 hPa). Próg wysokości dla pojawienia się objawów choroby dekompresyjnej (bez uprzedniej desaturacji) mieści się w dość dużym przedziale, od ok. 6 000 m n.p.m. (354 mm Hg - 472 hPa) do ok. 8 000 m n.p.m. (266 mm Hg - 365 hPa). Tak duży przedział wysokości wynika z różnych warunków i właściwości osobniczych ustroju poddanego działaniu dekompresji [4, 19]. Wśród czynników sprzyjających wystąpieniu objawów chorobowych, poza wielkością dekompresji i szybkością jej narastania, ma: czas przebywania w obniżonym ciśnieniu, wysiłek fizyczny, wiek, grubość tkanki tłuszczowej, temperatura oraz wrażliwość osobnicza.
Kliniczny przebieg wysokościowej choroby dekompresyjnej, choroby będącej klinicznym zespołem objawów związanych z uwolnieniem gazów, szczególnie azotu, w tkankach i płynach ustrojowych w wyniku obniżenia otaczającego ciśnienia atmosferycznego w znacznym stopniu określony jest:
- ilością pęcherzyków gazowych w ustroju,
- rozmiarami pęcherzyków gazowych,
- ich rozmieszczeniem,
- szybkością wzrostu pęcherzyków gazowych i ich zanikania [15]. Najczęściej występują (ponad 90% przypadków) bóle kostno-stawowe (bends).
Rzadziej pojawiają się takie dolegliwości, jak: mrowienie, parestezje, marmurkowatość czy też świąd skóry. Stwierdzono jednak, że objawy skórne poprzedzają zwykle ciężkie przypadki wysokościowej choroby dekompresyjnej (około 10 %), w której często występuje zapaść. Inne objawy rozwijającej się choroby dekompresyjnej, to uczucie duszności, poprzedzane zwykle kaszlem i bólami zamostkowymi (chokes). Zmiany zaś w układzie nerwowym objawiają się drgawkami klonicznymi, porażeniami połowicznymi, utratą przytomności i objawami lokalnych uszkodzeń różnych ośrodków kory mózgowej.
W zależności od stosowanych kryteriów, autorzy przedstawiają klasyfikacje różnych form wysokościowej choroby dekompresyjnej. Najczęściej spotyka się podział na trzy postacie [1, 6, 15, 20].
1. Lekką - za którą uznano postać z bólami mięśniowymi i bólami w okolicy stawów, w większości przypadków powstającymi podczas ruchów. Bóle te mogą ustąpić po pewnym czasie przebywania na wysokości lub zanikają przy „obniżaniu się" z wysokości. Do lekkich postaci zalicza się również przypadki, gdzie występują jedynie parestezje, marmurkowatość i świąd skóry (objawy te mogą jednak poprzedzać wystąpienie ciężkiej postaci choroby dekompresyjnej).
2. Średnia - postać, w której występują bóle w okolicy stawów (radiologicznie stwierdza się obecność pęcherzyków gazowych w tkance okołostawowej). Bóle narastają i rozszerzają się na okoliczne tkanki. Po powrocie do warunków normobarii bóle utrzymują się przez 2-3 h.
3. Ciężka - postać wysokościowej choroby dekompresyjnej charakteryzująca się bólami kostno-stawowymi „nie do zniesienia", bóle w klatce piersiowej, bóle zamostkowe, suchy kaszel, duszność.
Na podstawie objawów klinicznych dzieli się również chorobę dekompresyjną na:
a) postacie z łagodnym przebiegiem schorzenia (dolegliwości skórne, stawowe),
b) postacie o przebiegu złośliwym (bóle stawowe, mięśniowe, kostno-stawowe). W ciężkiej postaci wysokościowej choroby dekompresyjnej autorzy wyróżniają trzy postacie:
I. Postać płucną.
II. Postać z przewagą objawów neurologicznych.
III. Postać z zaburzeniami w układzie krążenia.
Postać płucna jest szczególnie niebezpieczna i często kończy się zapaścią. Liczne pęcherzyki gazowe w naczyniach krążenia płucnego, a także w samej tkance płucnej, powodują kaszel, bóle w klatce piersiowej i duszność (nasilającą się po napadach kaszlu), mogącą doprowadzić do utraty przytomności [6].
Objawy kliniczne postaci neurologicznej (ok. 25 % wszystkich postaci choroby dekompresyjnej przebiega z zaangażowaniem układu nerwowego) poza ogólnym osłabieniem, bólami głowy, drgawkami klonicznymi, to paraplegie, parestezje, afazje. Obserwuje się również spastyczność mięśni, utratę siły mięśniowej, nietrzymanie moczu i stolca oraz zaburzenia termoregulacji (hipertermia). Przy uszkodzeniu lub podrażnieniu nerwu wzrokowego występuje utrata pola widzenia, widzenie tunelowe, obraz za mgłą, zaś przy uszkodzeniu móżdżku lub opon mózgowych - zaburzenia koordynacji ruchowej, niezborność i drżenie zamiarowe, konfabulacje i zaburzenia osobowości [1].
Postać wysokościowej choroby dekompresyjnej z zaburzeniami w układzie krążenia, to masywne uszkodzenie śródbłonków naczyń przez pęcherzyki gazowe z następową utratą osocza oraz wpływ na ośrodek naczynioruchowy (postać nerwowo-krążeniowa, jedna z najcięższych postaci choroby dekompresyjnej), hipotonia, zapaść krążeniowa. Postaci tej towarzyszą silne bóle stawowe, duszność i często powikłania neurologiczne.
W piśmiennictwie często spotyka się określenie choroby dekompresyjnej jako „postać mieszana". Jest to postać wieloobjawowa, gdzie obok parestezji i mrowienia skóry występuje uczucie duszności, bóle stawów, hiperwentylacja, zawroty głowy i drgawki typu tężcowego. Zdarza się również, że choroba, początkowo określana jako „postać lekka", kończy się rozwojem pełnego obrazu postaci ciężkiej z zapaścią [11].
W piśmiennictwie opisywane są przypadki śmierci z powodu choroby dekompresyjnej, w czasie lotu na dużej wysokości. Adler H.P. (USAF Aviat. Med. 1955) opisując częstość występowania wysokościowej choroby dekompresyjnej u 1 000 000 pilotów badanych w komorach niskich ciśnień podaje 7 wypadków śmiertelnych, co stanowi 0,0007 % ogółu badanych (cyt. Za 11).
Wśród czynników usposabiających do powstawania wysokościowej choroby dekompresyjnej jest zwiększona masa ciała. Duża rozpuszczalność azotu w tkance tłuszczowej i jej małe ukrwienie warunkują wysokie prawdopodobieństwo tworzenia się w tkance tłuszczowej wolnych pęcherzyków gazowych. W przypadku uszkodzenia tkanki tłuszczowej, pęcherzyki gazowe wraz z drobinami tłuszczu mogą dostać się do naczyń i powodować w nich zatory. Czynnikiem warunkującym liczbę przypadków wysokościowej choroby dekompresyjnej jest też wiek.
Według danych z piśmiennictwa w poszczególnych grupach wiekowych stwierdzono:
-17-20 lat - 0,78% przypadków choroby,
-21-23 lata-1,6% przypadków choroby,
-24-26 lat - 4,98% przypadków choroby,
-27-29 lat - 7,43% przypadków choroby,
-30-35 lat - 5,99% przypadków choroby
Przypuszcza się, że jednym z powodów wzrostu liczby zachorowań jest zwiększająca się wraz wiekiem masa ciała. Bierze się również pod uwagę zmiany ukrwienia i lepszą desaturację ustroju z azotu w młodszym wieku. Wysiłek fizyczny powoduje również wzrost występowania objawów choroby dekompresyjnej. Pojawienie się dolegliwości bólowych w okolicy stawów tłumaczy się tym, że w okolicy aktywnych stawów okresowo pojawiają się miejscowe ogniska niskiego ciśnienia hydrostatycznego, ułatwiające tworzenie się pęcherzyków gazowych i ich zalążków 17]. W czasie pracy mięśniowej zwiększa się również ilość wytwarzanego dwutlenku węgla (ułatwiającego tworzenie się pęcherzyków gazowych). Wzrost temperatury pracujących mięśni powoduje, że pęcherzyki gazowe zwiększają swoją objętość.
Leczenie wysokościowej choroby dekompresyjnej
W przypadku wystąpienia objawów choroby dekompresyjnej podstawowym działaniem i podstawowym środkiem jest powrót do normobarii i rekompresja. Im krótszy jest czas od wystąpienia bólu do poddania badanego rekompresji, tym szybciej ustępują dolegliwości bólowe. Metoda rekompresji została podana w dalszej części rozdziału, istotne wydaje się omówienie na wstępie profilaktyki wysokościowej choroby dekompresyjnej.
Głównym czynnikiem patogennym jest azot w postaci gazowej. Usuwanie go z ustroju ze stanu rozpuszczenia ma największe znaczenie. Przy oddychaniu czystym tlenem, rozpuszczony w tkankach i płynach ustrojowych azot, przez nabłonek pęcherzyków płucnych przechodzi do powietrza pęcherzykowego i wydalany jest na zewnątrz. Zjawisko „wypłukiwania" azotu z ustroju nosi nazwę desaturacji. W piśmiennictwie eliminowanie azotu z ustroju określane jest również jako preoksygenacja. Często zamiennie używa się również terminu denitrogenacja [2, 13, 15, 19]. Najskuteczniejsza jest denitrogenacja na poziomie morza. Jak przedstawiono na rycinie 2, w zależności od rodzaju tkanki krzywa wydalania azotu z organizmu ma różny charakter. Ta różnorodna szybkość desaturacji zależy od współczynnika rozpuszczenia w nich azotu i stopnia ukrwienia tych tkanek. W ciągu pierwszej godziny oddychania czystym tlenem ustrój traci ok. 50% rozpuszczonego w tkankach azotu. Wynik desaturacji zależy jednak nie tylko od wielkości wydalonego azotu, lecz również i od tego, skąd i z jakich tkanek ten azot jest wydalany.
Duże znaczenie w profilaktyce wysokościowej choroby dekompresyjnej ma określenie czasu oddychania czystym tlenem w warunkach normobarii. Oczekiwaną wielkość profilaktycznego działania desaturacji określamy jako:
- minimalną,
- średnia,
- maksymalną.
Na rycinie 3 przedstawiono (wg 15) szybkość wydalania z ustroju azotu przy oddychaniu czystym tlenem, w różnych warunkach.
1 - oddychanie czystym tlenem w spoczynku.
2 – przy wysiłku fizycznym (określona ilość przysiadów),
3 - przy dowolnej hiperwentylacji,
4 - przy dodaniu do tlenu 3 % dwutlenku węgla.
W wyniku licznych prac stwierdzono, że oddychanie czystym tlenem w warunkach normobarii daje prawdopodobną wielkość obronną przed wystąpieniem choroby dekompresyjnej w ok. 30%. Oddychanie w tych warunkach przez godzinę to wielkość ok. 45%. Aby uzyskać prawdopodobną wielkość obronną ok. 90%. trzeba oddychać czystym tlenem 3,5-4 h. Poza działaniem profilaktycznym, jakim jest desaturacia ustroju z azotu przez oddychanie czystym tlenem lub innym gazem (np. hel, neon, rzadziej krypton), stosuje się również, zwłaszcza w medycynie kosmicznej, nieswoiste metody podwyższenia oporności na występowanie choroby dekompresyjnej [19]. Do najczęściej stosowanych należy zaliczyć kilkudniowe (7-10 dni), codzienne, poddawanie ludzi działaniu:
a) atmosfery hiperkapnicznej i normooksyjnej - 90 min. dziennie (pCO2 od 5.0-5,5 kPa),
b) hiperbarycznej oksygenacji - 45 min. raz dziennie (pO2 - 0,15 Mpa),
c) działaniu impulsów elektrycznych (wg Ł.K. Wołkowa i wsp. 1999 r., 19).
Metody te nie tylko, w sposób statystycznie istotny, podwyższają oporność ustroju na wystąpienie objawów choroby dekompresyjnej przy jednorazowym przebywaniu na wysokości. Oporność ta utrzymuje się przez kilka następnych dni (ok. 10). Nie należy przy tym zapominać, że trening fizyczny i dobra wydolność fizyczna określana maksymalnym poborem tlenu, jako metoda nieswoista, podnosi również oporność ustroju na występowanie choroby dekompresyjnej.
Ogólnie uważa się, że fenomen podwyższenia oporności ustroju na chorobę dekompresyjną określa się jako zjawisko adaptacji. W piśmiennictwie określa się, że:
1) można to przyrównać do wyników adaptacji sportowców do wysiłków fizycznych,
2) fenomen ten występuje, ponieważ przy powtórnym tworzeniu się pęcherzyków gazowych w tkankach zmniejsza się wrażliwość zakończeń nerwowych (w związku z pewną deformacją tkanek),
3) powtarzające się cykle kompresja-dekompresja prowadzą do zmniejszenia się ilości zarodków, wokół których tworzą się pęcherzyki azotu (do odtworzenia zarodków potrzeba pewnego czasu),
4) podwyższenie oporności (adaptacja) związane jest z usprawnieniem reakcji układu krążenia i układu oddechowego na powstawanie pęcherzyków gazowych. Stwierdzenia przedstawione w punktach 3 i 4 zostały w ostatnim czasie potwierdzone doświadczalnie [3, 4, 17, 19], Należy jednak zwrócić uwagę na fakt, że mało wiemy o liczbie pęcherzyków gazowych, które nie wywołują objawów choroby dekompresyjnej (bezobjawowe pęcherzyki gazowe). Stąd rozwój metody dopplerowskiej do wykrywania mikropęcherzyków pozwalających na ujawnienie stanu przedklinicznego. Brak objawów choroby dekompresyjnej nie wyklucza powstania w ustroju skrytych do jakiegoś czasu, negatywnych zjawisk [14].
Istnieje wiele wzorców leczenia choroby dekompresyjnej (opracowano specjalne tabele, stosowane w zależności od stanu chorobowego pilota). Jedną z metod jest poddawanie leczonego rekompresji w 100% atmosferze czystego tlenu w ciśnieniu 1 atm. Stosuje się również hiperbaryczną terapię tlenową w ciśnieniu 2 atm. Poza tlenoterapią stosuje się także leczenia farmakologiczne. Należy do nich steroidoterapia, środki sedatywne, kwas salicylowy, płyny infuzyjne. Należy dodać, że wszystkie przypadki średniej i ciężkiej postaci wysokościowej choroby dekompresyjnej należy bezwzględnie hospitalizować.
Autor: Lucjan GOLEC
Piśmiennictwo
1. Bishop J.A.: Effects of decreased pressure: Decompression sickness. USAF School of Aerospace Medicine. Flight Surgeon's Guide, 1989.
2. Boyle J.: Theoretical trans-respiratory pressures during rapid decompression. Aerospace Med., 1973, 44, 153-162.
3. Boussuges A., Succo E., Juhan-Vague I., Sainty J.M.: Activation of coagulation in decompression illness. Aviat. Space Eviron. Med., 1998, 69, 129-132.
4. Dart T.S., Buttler W.: Towards new paradigms for the treatment of hypobaric decompression sickness. Aviat. Space Environ. Med., 1998, 69, 403-409.
5. Davenport N.A.: Predictors of barotrauma events in a Navy altitude chamber. Aviat. Space Environ. Med., 1997, 68, 61-65.
6. DeHart R.L.: Decompression sickness and Pulmonary overpressure accidents. Fundamentals of Aerospace Medicine. William and Wilkins Comp., New York 1996, 357-411.
7. Fabian B.G.: Inflight decompression sickness affecting the temporomandibular joint. Aviat. Space Environ. Med., 1998, 69, 517-518.
8. Huszcza A.: Choroba kesonowa. Przeg. Bezp. Pracy. 1938, 5, 173-198.
9. Golec L., Sokołowski E.: Wpływ nagłej dekompresji na ustrój. Post. Astronautyki, 1968, 2, 95-105.
10.Jethon Z.: Patogeneza i klinika choroby dekompresyjnej. Zbiór prac WIML, Warszawa 1960, 5, 18-34.
11. Katuncew W.P.: Dekompresjonnaja bolezń - adna iz aktualnych problem awiakosmiczeskoj medicyny. Aviakosm. Ekołog. Med., 1998, 32, 11-19.
12. Krzyżak J.: Patofizjologia choroby ciśnieniowej nurków. Pol. Tyg. Lek., 1985, 40, 1054-1058.
13.Krzyżak J.: Leczenie choroby ciśnieniowej i zatorów powietrznych. Pol. Tyg.Lek. 1987, 6. 42. 171-176.
14.Kumar V.K., Billica R.D., Waligóra J.M.: Utility of Doppler-detectable micro bubbles in the diagnosis and treatment of decompression sickness. Aviat. Space Environ. Med., 1997, 67, 151-157.
15. Małkin W.B.: Ciśnienie barometryczne. Skład gazowy. Inf. Lotn.-Lek. (tłumaczenie wyd. spec.), Warszawa 1982, 6-31.
16. Sokołowski E., Golec L., Błaszczakiewicz M.: Wpływ nagłej dekompresji na niektóre odczyny ustroju pilota. Med. Lotn., 1971, 33, 75-82.
17. Webb J.T., Pilmanis A.A., O'Connor R.B.: Preoxygenation altitude threshold for decompression sickness symptoms. Aviat. Space Environ. Med., 1998, 68, 335-340.
18. Wojciechowicz I.A.: Kompleksnaja matematiczeskaja model dekompresii, asnowannaja na biofizyczeskich i fizjołogiczeskich zakomomiernostijach. Aviakosm. Ekołog. Med., 1996, 30, 2, 37-43.
19. Wołkow L.K., Miasnikow Ał.A., Miasnikow An.A., Sonin L.N., Bojko J.G.: Ustoicziwost ludiej k dekompresjonnoj bolezni i niespecyficzeskije metody jejo powyższenija. Aviakosm. Ekołog. Med., 1999, 33, 3, 40-43.
20.Wood R.H., Sweginis R.W.: Aircraft accident investigation. Endeavour Books, 1995, 155-161.





















